课题组工作丨ANGEW丨胰岛素样生长因子2-核酸适体嵌合体用于高效降解多种靶标膜蛋白
在恶性肿瘤的发生发展过程中,致病膜蛋白的高表达是肿瘤细胞快速增殖和转移的关键驱动力[1]。针对膜蛋白的小分子抑制剂和单克隆抗体阻断剂的开发与应用在癌症治疗方面取得了巨大成功[2]。然而,目前这些干扰膜蛋白功能的方法仍面临成本高、结果不可预测和效率低等挑战[3]。近年来,科研人员进一步开发了一种靶向膜蛋白降解技术,利用异源双功能分子高效、快速、特异性地降解致病膜蛋白,特别是针对传统上的不可成药蛋白,引起了广泛关注。
近日,韩达研究员团队在《Angew. Chem. Int. Ed.》杂志在线发表了题为“Insulin-like Growth Factor 2-Tagged Aptamer Chimeras (ITACs) Modular Assembly for Targeted and Efficient Degradation of Two Membrane Proteins”的工作。
本课题组提出了一种利用细胞膜表面溶酶体穿梭循环受体蛋白(胰岛素样生长因子2受体,IGF2R)降解靶标膜蛋白的策略,实现了多种致病细胞膜蛋白的快速高效降解。我们将胰岛素样生长因子2(IGF2)与核酸适体相结合,构建了IGF2-核酸适体嵌合体(ITACs)。其中,核酸适体能够高特异性高亲和力地结合靶标膜蛋白,而IGF2可被细胞膜表面IGF2R识别、摄取并转运至溶酶体。因此,ITACs能够将核酸适体结合蛋白转运至溶酶体中,进行快速高效的靶向降解。作为概念验证性实验,我们首先通过流式细胞术和共聚焦显微成像术,明确修饰有随机序列DNA的IGF2依然可被IGF2R表达的细胞结合、摄取并转运至溶酶体。


模式图:ITACs介导的细胞膜蛋白靶向降解


图1. ITACs-RS可与细胞结合并被内吞。(A)模式图;(B-C)ITACs-RS可与膜表面表达IGF2R的细胞结合;(D)ITACs-RS可被细胞内吞并转运至溶酶体。
进一步,我们将IGF2蛋白与靶向细胞间质上皮转换因子(MET)的核酸适体共价连接,构建ITACs-MET嵌合体,利用免疫印迹、流式细胞术、免疫荧光成像等细胞生物学技术,我们明确ITACs-MET介导细胞膜MET蛋白经IGF2R/溶酶体途径讲解。类似的,我们构建了ITACs-PTK7、ITACs-EpCAM和ITACs-FGFR2嵌合体,明确ITACs平台可在多个细胞系中实现细胞膜表面多种靶标蛋白的溶酶体转运和降解。


图2. ITACs-MET介导细胞膜表面c-MET经溶酶体降解。(A)模式图;(B-F)ITACs-MET对c-MET蛋白的降解呈现浓度和时间梯度的依赖;(G-H)ITACs-MET介导c-MET蛋白溶酶体转运。


图3. ITACs-PTK7、ITACs-EpCAM和ITACs-FGFR2b分别介导细胞膜表面PTK7、EpCAM和FGFR2经溶酶体降解。(A-C)ITACs-PTK7、ITACs-EpCAM和ITACs-FGFR2b介导PTK7、EpCAM和FGFR2蛋白降解;(D-E)ITACs-PTK7介导PTK7溶酶体转运;
为探究ITACs嵌合体在不同细胞系对膜蛋白MET和PTK7的降解效率,我们利用流式细胞术和蛋白免疫印迹实验,明确ITACs对靶蛋白的降解效果与细胞膜表面IGF2R丰度有关,即在IGF2R表达适中的细胞系中ITACs对靶蛋白的降解效果较好,而在IGF2R高表达的细胞系中ITACs几乎对靶蛋白无效。


图4. ITACs介导的膜蛋白靶向降解效率和膜表面IGF2R丰度的关系。(A)ITACs-MET对MCF7和SK-BR-3细胞中的c-MET没有降解效果;(B)各c-MET高表达细胞系中膜表面IGF2R蛋白表达水平:(C)各细胞膜表面IGF2R水平和c-MET蛋白降解效率的关系;(C)ITACs-PTK7对CCRF-CEM和SK-BR-3细胞中的PTK7没有降解效果;(E)各PTK7高表达细胞系中膜表面IGF2R蛋白表达水平:(F)各细胞膜表面IGF2R水平和PTK7蛋白降解效率的关系。
最后,我们建立了一种模块化组装策略,在一个IGF2蛋白分子上同时修饰靶向不同膜蛋白的两种核酸适体,实现了多种靶标膜蛋白的同时降解,并且产生了1+1>2的降解效果,为有效降解疾病相关膜蛋白提供了新技术,为重大疾病的治疗提供了新思路和新方法。
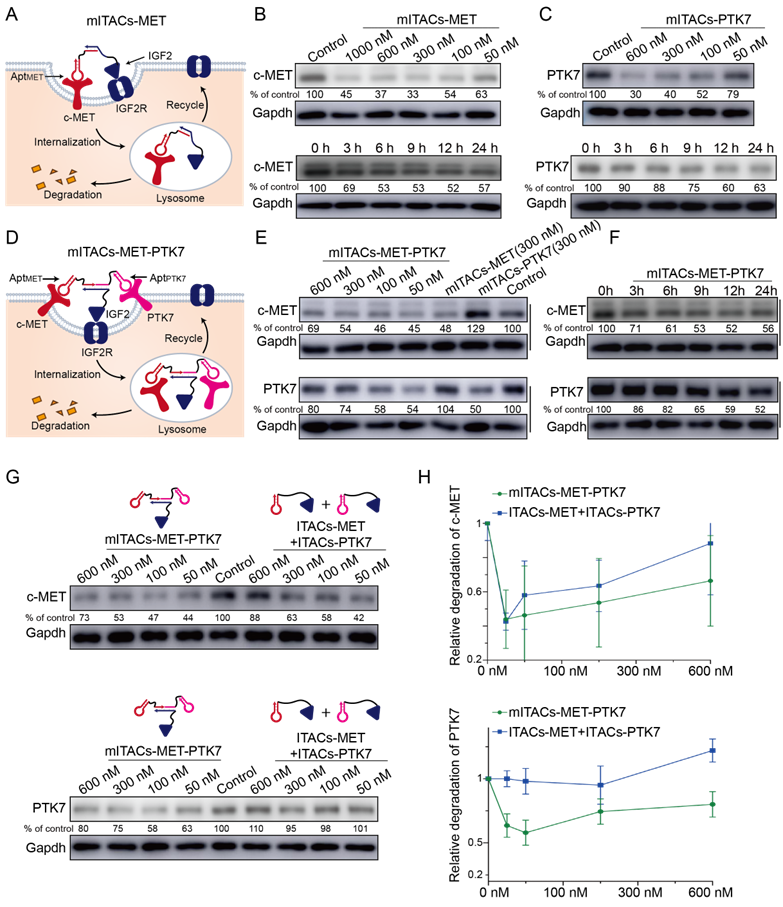

图5. mITACs介导的双膜蛋白同时降解。(A)模式图;(B-C)模块化组装的mITAC-MET和mITAC-PTK7可分别接到c-MET和PTK7蛋白降解;(D)模式图;(E-F)mITAC-MET-PTK7介导c-MET和PTK7同时降解;(G-H)mITAC-MET-PTK7与ITACs-MET+ITACs-PTK7对c-MET和PTK7同时降解的效率比较。
论文信息:
[1] Y. Tian, Y. Miao, P. Guo, J. Wang, D. Han, Angew. Chem. In.t Ed. 2023, e202316089.
https://doi.org/10.1002/anie.202316089
参考文献:
[1] aG. da Cunha Santos, F. A. Shepherd, M. S. Tsao, Annual Review of Pathology: Mechanisms of Disease 2011, 6, 49-69; bB. Peruzzi, D. P. Bottaro, Clinical cancer research 2006, 12, 3657-3660.
[2] aT. Martens, N.-O. Schmidt, C. Eckerich, R. Fillbrandt, M. Merchant, R. Schwall, M. Westphal, K. Lamszus, Clinical cancer research 2006, 12, 6144-6152; bP. C. Ma, E. Schaefer, J. G. Christensen, R. Salgia, Clinical cancer research 2005, 11, 2312-2319.
[3] M. Békés, D. R. Langley, C. M. Crews, Nature Reviews Drug Discovery 2022, 21, 181-200.

